УГЛЕВОДЫ
обширная группа органических
соединений, входящих в состав всех живых организмов. Первые известные представители
этого класса веществ по составу отвечали общей формуле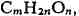
т. е. углерод + вода (отсюда назв.); позднее к У. стали относить
также их многочисленные производные с иным составом, образующиеся при окислении,
восстановлении или введении заместителей.
Превращения У. известны с древнейших времён,
т. к. они лежат в основе процессов брожения, обработки древесины, изготовления
бумаги и тканей из растит. волокна. Тростниковый сахар (сахарозу) можно
считать первым органич. веществом, выделенным в химически чистом виде.
Химия У. возникла и развивалась вместе с органической химией; создатель
структурной теории органич. соединений А. М. Бутлеров - автор первого
синтеза сахароподобного вещества из формальдегида (1861). Структуры
простейших Сахаров выяснены в кон. 19 в. в результате фундаментальных исследований
нем. учёных Г. Килиани и Э. Фишера, основанных на стереохимич. представлениях
Я. Г. Вант-Гоффа и блестяще их подтвердивших. В 20-е гг. 20 в. работами
англ. учёного У. Н. Хоуорса были заложены основы структурной химии полисахаридов.
Со 2-й пол. 20 в. происходит стремительное развитие химии и биохимии У.,
обусловленное их важным биол. значением и базирующееся на совр. теории
органич. химии и новейшей технике эксперимента.
Классификация и распространение углеводов.
У. принято делить на три осн. группы: моносахариды, олигосахариды и полисахариды.
Обычные моносахариды представляют собой полиоксиальдегиды (альдозы)
или
полиоксикетоны (кетозы) с линейной цепью атомов углерода (m = 3-9),
каждый из к-рых (кроме карбонильного углерода) связан с гидроксильной
группой. Простейший из моносахаридов - глицериновый альдегид - содержит
один асимметрический атом углерода и известен в виде двух оптических антиподов
(D и L). Прочие моносахариды имеют неск. асимметрических атомов
углерода; их рассматривают как производные D- или L-глицеринового альдегида
и относят в соответствии с абсолютной конфигурацией при (т-1)-м
атоме углерода к D- или L-ряду. Различия между моносахаридами в каждом
ряду обусловлены относительной конфигурацией остальных асимметрических
центров (см. Изомерия). Характерное свойство моносахаридов в растворах
- способность к мутаротации, т. е. установлению таутомерного равновесия
(см. Таутомерия) между ациклической альдегидо- или кетоформой, двумя
пяти-членными (фуранозными) и двумя шестичленными (пиранозными)
циклич. полу-ацетальными формами (см. схему). Образующиеся пиранозы (как
и фуранозы) различаются конфигурацией (а или Р) возникающего при циклизации
асимметрического центра у карбонильного атома углерода (на схеме помечен
звёздочкой).
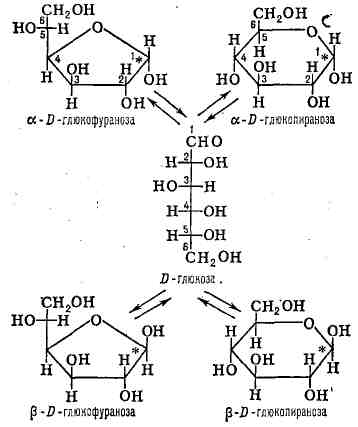
Соотношение между таутомерными формами
в равновесии определяется их термодинамической устойчивостью (для обычных
Сахаров преобладают пиранозные формы). Полуацетальный гидроксил
резко отличается от прочих гидроксильных групп моносахарида по способности
к реакциям нуклеофильного замещения. Такие реакции с разнообразными спиртами
приводят к образованию гликозидов (остаток спирта в гликозиде наз.
агликоном). В тех случаях, когда агли-коном служит молекула моносахарида,
образуются олиго- и полисахариды. При этом каждый остаток моносахарида
может иметь пиранозную или фуранозную структуру, альфа- или бетта-конфигурацию
гликозидной связи и быть связанным с любой из гидроксильных групп соседнего
моносахарида. Поэтому число различающихся строением полимерных молекул,
к-рые можно построить даже только из одного моносахарида, огромно.
К наиболее типичным моносахаридам относятся
D-глюкоза, D-манноза, D-галактоза, D-фруктоза,
D-ксилоза, L-арабиноза. К моносахаридам относятся также:
дезоксисахара, в молекулах к-рых один или неск. гидроксилов заменены атомами
водорода (L-рамноза, L-фукоза, 2-дезокси-D-рибоза); аминосахара,
в молекулах к-рых один или неск. гидроксилов заменены на аминогруппы (D-глюкозамин,
D-галактозамин); многоатомные спирты, или альдиты, образующиеся
при восстановлении карбонильных групп моносахаридов (сорбит, маннит);
урановые
кислоты, т. е. моносахариды, у к-рых первичная спиртовая группа окислена
до карбоксильной; разветвлённые сахара, содержащие нелинейную цепь углеродных
атомов (апиоза, L-стрептоза); высшие сахара с длиной цепи более
шести атомов углерода (седогептулоза, опаловые кислоты).
За исключением
D-глюкозы и D-фруктозы, свободные моносахариды встречаютсяв природе редко.
Обычно они входят в состав разнообразных гликозидов, олиго-и полисахаридов
и могут быть получены из них кислотным гидролизом. Разработаны методы химич.
синтеза редких моносахаридов, исходя из более доступных.
Олигосахариды содержат в своём составе
2-10 моносахаридов, связанных гликозидными связями. Наиболее распространены
в природе дисаха-риды сахароза, трегалоза, лактоза. Известны многочисленные
гликозиды оли-госахаридов, к к-рым относятся различные физиологически активные
вещества (напр., флавоноиды, сердечные гликозиды, сапонины, мн.
антибиотики, гли-колиииды).
Полисахариды - высокомолекулярные, линейные
или разветвлённые соединения, молекулы к-рых построены из моносахаридов,
связанных гликозидными связями. В состав полисахаридов могут входить также
заместители неуглеводной природы (остатки фосфорной, серной и жирных к-т).
В свою очередь цепи полисахаридов могут присоединяться к белкам с образованием
гликопротеидов.
Отд. группу составляют биополимеры, в молекулах к-рых остатки моно-
или олигосахаридов соединены друг с другом не гликозидными, а фосфодиэфирными
связями; к этой группе относятся тейхоевые к-ты из клеточных стенок грамположительных
бактерий, нек-рые полисахариды дрожжей, а также
нуклеиновые кислоты,
в основе к-рых лежит полирибозофосфатная (РНК)
или поли-2-дезоксирибозофосфат-ная
(ДНК) цепь.
Физико-химические свойства углеводов.
Благодаря обилию полярных (гидроксильных, карбонильной и др.) групп
в молекулах моносахаридов они хорошо растворимы в воде и нерастворимы в
неполярных органич. растворителях (бензоле, петролейном эфире и др.).
Способность к таутомерным превращениям обычно затрудняет кристаллизацию
моносахаридов. Если такие превращения невозможны, как в гликозидах или
оли-госахаридах типа сахарозы, вещества кристаллизуются легко. Мн. гликозиды
с малополярными агликонами (напр., сапонины) проявляют свойства
поверхностно-активных соединений. Полисахариды являются гидрофильными полимерами,
молекулы к-рых способны к ассоциации с образованием высоковязких растворов
(растит. слизи, гиалуроновая кислота); при определённом соотношении
свободных и ассоциированных участков молекул полисахариды дают прочные
гели
(агар, пектиновые вещества). В отд. случаях молекулы полисахаридов
образуют высокоупорядоченные надмолеку-лярные структуры, нерастворимые
в воде (целлюлоза, хитин).
Биологическая роль углеводов. Роль
У. в живых организмах чрезвычайно многообразна. В растениях моносахариды
являются первичными продуктами фотосинтеза и служат исходными соединениями
для биосинтеза разнообразных гликозидов, полисахаридов, а также веществ
др. классов (аминокислот, жирных к-т, полифенолов и т. д.). Эти
превращения осуществляются соответствующими ферментными системами, субстратами
для к-рых служат, как правило, богатые энергией фосфорилированные производные
Сахаров, гл. обр. нуклеозиддифосфатсахара. У. запасаются в виде крахмала
в
высших растениях, в виде гликогена в животных,< бактериях
и грибах и служат энергетическим резервом для жизнедеятельности организма
(см. Брожение, Гликолиз, Окисление биологическое). В виде гликозидов
в растениях и животных осуществляется транспорт различных продуктов обмена
веществ. Многочисл. полисахариды или более сложные углеводсодер-жащие полимеры
выполняют в живых организмах опорные функции. Жёсткая клеточная стенка
у высших растений построена из целлюлозы и гемицеллюлоз, у бактерий - из
пептидогликана; в построении клеточной стенки грибов и наружного скелета
членистоногих принимает участие хитин.
В организме животных и человека опорные
функции выполняют сульфатированные мукополи-сахариды соединительной
ткани, свойства к-рых позволяют обеспечить одновременно сохранение формы
тела и подвижность отд. его частей; эти полисахариды также способствуют
поддержанию водного баланса и избирательной катион-ной проницаемости клеток.
Аналогичные функции в мор. многоклеточных водорослях выполняют сульфатированные
галактаны (красные водоросли) или более сложные сульфатированные
гетерополисахариды (бурые и зелёные водоросли); в растущих и сочных
тканях высших растений аналогичную функцию выполняют пектиновые вещества.
Особенно важную и до конца ещё не изученную роль играют сложные У. в образовании
специфич. клеточных поверхностей и мембран. Так, гликолипиды - важнейшие
компоненты мембран нервных клеток, липополисахариды образуют наружную оболочку
грамотрицательных бактерий. У. клеточных поверхностей часто определяют
явление иммунологической специфичности, что строго доказано для групповых
веществ крови и ряда бактериальных антигенов. Имеются данные, что
углеводные структуры принимают участие также в таких высокоспецифичных
явлениях клеточного взаимодействия, как оплодотворение, "узнавание" клеток
при тканевой дифференциации и отторжении чужеродной ткани и т. д.
Практическое значение углеводов.
У. составляют большую (часто основную) часть пищевого рациона человека
(см. Питание). В связи с этим они широко используются в пищевой
и кондитерской пром-сти (крахмал, сахароза, пектиновые вещества, агар).
Их превращения при спиртовом брожении лежат в основе процессов получения
этилового спирта, пивоварения, хлебопечения; др. типы брожения позволяют
получить глицерин, молочную, лимонную, глюконовую к-ты и др. вещества.
Глюкоза, аскорбиновая кислота, сердечные гликозиды, углевод-содержащие
антибиотики, гепарин широко применяются в медицине. Целлюлоза служит основой
текст, пром-сти, получения искусств. целлюлозного волокна, бумаги,
пластмасс (см. Этролы), взрывчатых веществ (см. Нитраты целлюлозы)
и
др.
Важнейшие вопросы химии и биохимии У.-
усовершенствование методов установления строения и синтеза природных У.,
выяснение связи между их структурой и функцией в организме, а также путей
биосинтеза - разрабатываются химич. и биохимич. науч. центрами наряду с
др. актуальными проблемами органич. химии, биохимии и молекулярной биологии.
Исследованиям только в области У. посвящены специализированные междунар.
издания: ежегодник "Advances in Carbohydrate chemistry and biochemistry"
(с 1945) и журн. "Carbohydrate research" (c 1965). См. также
статьи Брожение, Соединения природные, Углеводный обмен, Фотосинтез.
Лит.: Химия углеводов, М., 1967;
Методы химии углеводов, пер. с англ., М., 1967; Гли-копротеины [т. 1 -
2], пер. с англ., М., 1969; Carbohydrates, ed. by G. О. Aspinall, L.- Baltimore,
[1973]; Industrial gums, eds. R. L. Whistler and J. N. Beiruller, 2 ed.,
N. Y.- L., 1973- А. И. Усов.
А Б В Г Д Е Ё Ж З И Й К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Ъ Ы Ь Э Ю Я